시장의 수용(acceptance) 속도에 주목해야 할 시기
KISTI 산업시장분석실 책임연구원 김유일 (Tel: 02-3299-6026 e-mail: yekim@kisti.re.kr)
| [ 요약 ] 1. 바이오시밀러 시장은 성장호르몬, 에리트로포이에틴, 필그라스팀 제품들로 구성되어 있으며, 2012년 현재 8.8억 달러로 성장하였다. |
제품개요
바이오시밀러는 식품의약품안정청의 정의에 따르면, “이미 제조판매·수입품목 허가를 받은 품목 (reference drug)과 품질 및 비임상·임상적 비교동등성(comparability)이 입증된 생물의약품”이다.
바이오시밀러는 다양한 다른 이름도 있으나, 광의의 바이오시밀러와 협의의 바이오시밀러로 구분할 수 있다. 광의의 바이오시밀러(<그림1>에서 Non Originals)는 판매독점권이 풀린 오리지널 생물의약품에 대비되는 바이오제너릭 제품으로 볼 수 있으며, 협의의 바이오시밀러(<그림1>에서 Biosimilars)는 EU, 일본, 우리나라와 같이 별도의 임상기준을 제시하고 이를 만족시키는 제품을 일컫는다.
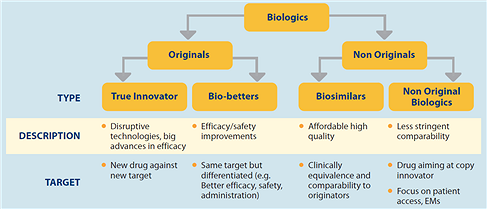
<그림 1> 생물의약품 분류
자료 : IMS Health, 2013, "Searching for Terra Firma in the Biosimilars and Non-Original Biologics Market"
제너릭 의약품과는 달리, 바이오시밀러는 보다 엄격한 임상을 요구한다. 임상을 거쳐야 하기 때문에 바이오시밀러 제품을 출시하기 위해서는 긴 시간(6~10년)과 많은 비용(1~2억 달러)이 필요하며, 이에 따라 기업은 기술력 뿐 아니라 자본력까지 갖추어야 한다.
시장동향 및 예측
바이오시밀러 시장은 2009년에 2.4억 달러에서 2012년에는 8.8억 달러로 매년 53.4%씩 매우 가파르게 성장하고 있다. 이러한 상승세는 일정기간 지속될 전망이며, 2016년에는 79.1억 달러까지 성장하여 2012년 이후 연평균 73.4%의 성장이 예상되고 있다. 성장세는 미국시장의 성장, 기존 제품에 대한 지식과 임상경험의 증가에 따른 시장수용의 증가, 신규 제품의 지속적인 진출 등에 따른 것으로 해석된다.
지역별로 보면 유럽이 전체시장의 44%로, 중국 13.2%, 미국 12.3%, 한국 8%, 인도 6.7% 등의 지역보다 시장규모도 크고 빠르게 가이드라인을 제시하면서 시장을 선도하고 있는 것으로 나타났다. 이는 일반 바이오 의약품 시장과는 차이를 보인다. 바이오 의약품 시장의 거의 절반은 미국시장이고 약 20%가 유럽시장이다. 바이오 의약품 시장의 성장을 견인하는 것도 미국이 거의 절반을 차지한다. 그러나 미국이 바이오시밀러에 대한 태도를 유보함에 따라 비중이 적었지만 미국의 바이오시밀러에 대한 태도가 점차 구체화됨에 따라 시장규모와 시장성장에 많은 기여를 할 것으로 전망하고 있다.
<표 2> 바이오시밀러 시장규모 전망 (단위 : 백만달러)
| 년도 개요 | 시장 규모 | CAGR | ||||
| 2012 | 2013(E) | 2014 (F) | 2015(E) | 2016 (E) | ||
| 세계 시장 | 876.1 | 1,197.9 | 1,663.8 | 5,008.7 | 7,912.4 | 73.4% |
자료 : Frost & Sullivan, 2014.1, "Analysis of the Global Biosimilars Market"
※ 참고 : IMS Health 자료는 바이오시밀러 시장이 2012년에 24.8억 달러의 규모이며, 2020년에는 110~250억 달러까지 성장할 것으로 전망하고 있음.(동 기간동안 CAGR, 21~34%)
시장경쟁상황
전 세계적으로 바이오시밀러 시장은 Sandoz사가 38% 가량 점유하면서 선도적인 위치를 차지하고 있다. 상위에 랭크되어 있는 Sandoz, Teva, Hospira, STADA, Medice 등은 모두 제너릭 의약품이나 바이오시밀러를 전문으로 하는 기업들이다.
현재 수십개의 회사들이 시장에 참여하고 있으며, 이들은 제너릭 의약품 기업, 바이오 의약품 기업, 다국적 제약회사들이다. 거대 다국적 제약회사로는 Eli Lilly, Merck, Pfizer, AstraZeneca가 바이오시밀러 시장에 참여하고 있으며, 바이오 의약품 회사로는 우리나라의 셀트리온을 포함하여 Cangene, Reliance Life Sciences, Biocon, Biopartners 등이 있다. 기존에 제약과 상관없던 기업 중에서도 바이오시밀러 참여를 시작한 회사들도 있다. 이 회사들 중에 삼성전자와 후지필름이 눈에 띄는데, 삼성전자는 CRO 기업인 Quintiles와 바이오텍 기업인 Biogen Idec사와 협력하여 바이오시밀러 합작회사를 설립하는 방식을 취하고 있다. 후지필름의 경우는 일본의 Kyowa Kakko Kirin과 50대 50으로 바이오시밀러 개발을 위해 조인트 벤처를 설립하는 계약을 2012년에 체결하였다.
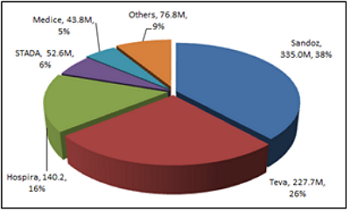
자료 : Frost & Sullivan, 2014.1, "Analysis of the Global Biosimilars Market", KISTI 재작성
참고 : Sandoz는 Hexal, Teva는 Ratiopharm과 CT Arzneimittel를 포함한 점유율임.
우리나라 바이오기업들이 오래전부터 복제-바이오 의약품을 생산해오고 있었고, 셀트리온의 항체 바이오시밀러에 대한 EMA의 품목허가와 삼성전자의 바이오시밀러 시장참여 등으로 국내 바이오시밀러에 대한 관심이 매우 높다. 바이오시밀러 제품이 시장에서 성공하기 위해서는 품목의 허가(approval)도 중요하지만 의사나 환자에게 수용(acceptance)되어야 한다. 또한, 수요층에서 수용정도가 커지면 점차 일반제품화 되면서 가격경쟁력을 가져야만 성공할 수 있게 될 것이다.
지금은 정부 당국과 약품의 수요층이 제너릭 의약품을 받아들이고 있지만, 제너릭의약품은 1984년 미국에서 출시가능해진 이후 벌써 30년이란 시간이 지났다. 바이오시밀러가 시장에 출시된 지 7년이 지난 2013년 기준으로 바이오시밀러가 바이오 의약품에 차지하는 비중은 고작 1.4% 정도로 보고되고 있어 매우 더딘 수용정도를 보이고 있으나 성장가능성은 크다. 하지만 중요한 것은 얼마나 빠르게 수용정도가 증가할 것인가에 있다.
지난 7년간의 EU 시장에서 국가별 바이오시밀러 수용정도는 차이를 보이고 있다. 바이오시밀러의 최대기업인 Sandoz가 있는 독일의 경우 바이오시밀러 시장 초기부터 비교적 높은 수용정도를 보인, 반면 프랑스, 이탈리아나 스페인의 경우는 유럽의 재정위기가 본격적으로 시작되기 바로 전인 2009년부터 수용정도가 빠르게 증가하기 시작하였다. 수요자의 지불비중 보다 국가나 보험의 지불비중이 높은 선진시장의 경우, 글로벌 경제위기나 재정위기 등이 바이오시밀러 수용속도에 영향을 줄 가능성이 크다. 예를 들어 이탈리아의 AIFA(Azengia Italiana del FArmaco, Italian Medicines Agency)가 최근 발간한 보고서에서는 바이오시밀러에 대해 긍정적인 의견을 피력하였으며, 의료비용 절감에 바이오시밀러의 역할을 강조하였다. 또한, 대체 조제에 대한 허용여부를 각국에 따라 결정할 수 있게 되어 있는 EU에서 2014년 2월 프랑스가 최초로 바이오시밀러 대체조제를 허용하기도 하였다.
하지만, 의료비용의 부담에 따른 정부차원의 바이오시밀러 수용 확대 방향은 바이오시밀러 약가 인하와 연계될 가능성이 커진다는 측면도 함께 가지고 있다.
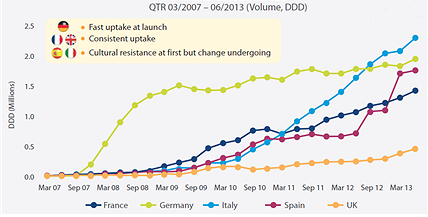
자료 : IMS Health, 2013, "Searching for Terra Firma in the Biosimilars and Non-Original Biologics Market"
비록 시장규모와 성장속도는 바이오시밀러 시장이 크긴 하지만, 항체나 인슐린 바이오시밀러의 경우 중증의 만성질환을 대상으로 하고 있어, 의사 입장에서는 장기간의 임상결과가 바이오시밀러를 안심하고 선택할 수 있는 정보이기 때문이다. 그리고 항암제나 당뇨병 대상 바이오시밀러 시장는 시장이 큼에도 불구하고 현재까지의 수용정도가 매우 낮은 편이기 때문에 빠른 임상결과의 축적은 수용속도를 가속화 하는 중요한 요소로 작용할 수 있다.
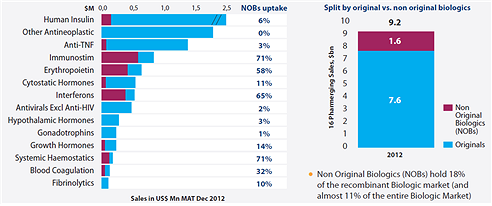
자료 : IMS Health, 2013, "Searching for Terra Firma in the Biosimilars and Non-Original Biologics Market"

